Western Blot
蛋白免疫印跡(Western Blot)在醫學科研中應用非常廣泛,是非常基礎的分子生物學技術。Western blot是將電泳分離后的細胞或組織總蛋白質從凝膠轉移到固相支持物NC膜或PVDF 膜上,然后用特異性抗體檢測某特定抗原的一種蛋白質檢測技術,現已廣泛應用于基因在蛋白水平的表達研究、抗體活性檢測和疾病早期診斷等多個方面。
實驗步驟
一、蛋白提取
1. 融解RIPA裂解液,混勻。取適當量的裂解液,在使用前數分鐘內加入PMSF,使PMSF的最終濃度為1mM.
2.去除細胞培養液,用PBS、生理鹽水或無血清培養液洗一遍(如果血清中的蛋白不干擾后續實驗,可以不洗)。以六孔板每孔加入150-250微升裂解液的比例加入裂解液。用移液器反復吹打,使細胞和裂解液充分接觸。
3.將細胞裂解液轉移至1.5mL的離心管中,置于冰上放置30min,每隔10min vortex一次,使細胞裂解充分;4℃10000-14000g離心10min,取上清,即可進行后續的蛋白電泳操作。
二、BCA法測樣本中蛋白含量
取A液和B液以50:1的比例混勻,96孔板每孔加入200μl,
另用標準品做一標準曲線,濃度梯度如下:
2000、1000、500、250、125、62.5、31.25、15.625μg/ml;
每孔加入標準品或樣品20μl,37 ℃孵育30 min,酶標儀檢測樣品在562 nm波長下的吸光值并計算出相應蛋白濃度(μg/μL),乘以樣品稀釋倍數即為樣品實際濃度(單位:μg /μL),根據樣品濃度確定上樣量。
三、蛋白印記法測蛋白含量
1. 將蛋白液與5X loading buffer一起混勻后,放入100℃金屬浴5-6min.放置冰上,待上樣。
2. 準備配制SDS-PAGE分離膠。
選擇10%的分離膠按順序加各溶液,混勻好,加入兩塊制膠玻璃板中,用水封平。待下層膠凝固后,將水倒掉,吸干,開始配制濃縮膠。
按順序加各溶液,混勻好,加入兩塊制膠玻璃板中,不要有氣泡,立即將梳子插入,凝固后將梳子拔出。
做好制膠槽后,放在冰上,將電泳buffer倒入后,開始上樣,每個孔上樣40μg.記錄上樣次序。
事先配制Running buffer【tris 3.028g(25mM),Gly 14.413g(192mM),10% SDS 10mL(0.1% SDS),用ddH2O定容至1000mL】,需放在4℃預冷。
Transfer buffer 【tris 3.028g (25mM),Gly 14.413g(192mM),甲醇(Methanol) 100mL用ddH2O定容至1000mL】,需放在4℃預冷。
4. 上層膠60v,30min;下層膠100v,90min.電泳結束后需要將膠放在PBS潤洗2min,再放入轉膜緩沖液中浸泡平衡。
5. 將剪好的PVDF膜先在甲醇中浸泡5min,后在ddH2O中浸泡2min,最后在transfer buffer 中浸泡平衡15min.
6. 墊子、膜和膠的放置:紅、(+)白架子、墊子、濾紙、膜、膠、濾紙、墊子、黑架子、黑(-)。轉膜條帶是從-到+.
7. 冰上轉移,200mA恒流轉膜,根據蛋白分子量大小確定轉膜時間。轉移結束后將膜放入PBS中浸泡3-5min,剪膜。
8. 用5%脫脂牛奶(0.75g奶粉+15mL PBS)在37℃封閉1-2h.
9. 洗膜,1×PBS-T(1000mL 1×PBS+1mL Tween-20) 5-10 min,三次。
10. 孵育一抗(Hexokinase 1,1:1000稀釋;NOS3,1:200稀釋;ACSS2,1:1000稀釋;NSE/ENO2,1:1000稀釋;β-actin,43kDa,1:1000稀釋),以上抗體均用5%脫脂牛奶稀釋,4℃ 孵育過夜。
11. 從冰箱中取出膜,洗膜,1×PBST 5 min/次,6次。
12. 加二抗(鼠抗,1:5000;兔抗,1:10000),37℃,2h,搖床。
13. 洗膜,1×PBST 5 min/次,6次。
14. 化學發光顯影 (Millipore ECL system)。
15. 結果分析(Tanon, TanonImage) 記錄、拍照、掃描和保存。
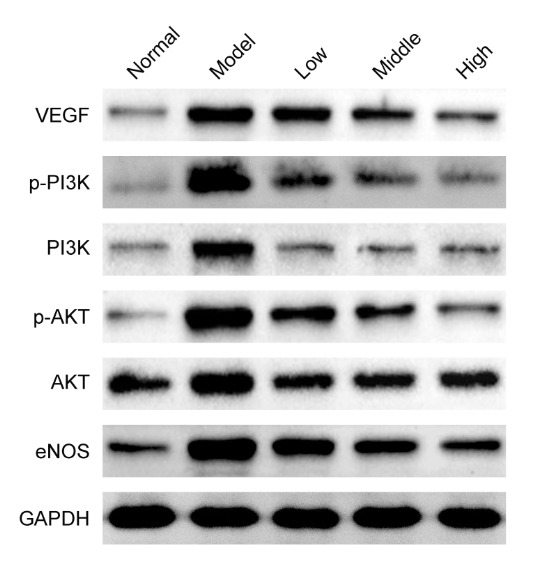
結果示例
Western blot
上一篇:沒有了
下一篇:實時熒光定量PCR
下一篇:實時熒光定量PCR






